2021年10月23日,第五届国际肿瘤精准医疗大会在北京朝阳悠唐皇冠假日酒店圆满结束。来自临检中心/中检院/临床/头部产业等50余位肿瘤精准领航人,与600余位专业听众齐聚一堂,围绕肿瘤精准诊疗,从防到诊到治,从早期筛查、分期分型、预后检测、伴随诊断、生物标志物、精准免疫/靶向药物开发及转化等方面,展开了深入的探讨分享。

裕泰抗原总经理苏小凡博士应邀在“肿瘤创新药物疗法与标志物/伴随研究的精准开发转化论坛”进行相关报告,阐述了如何围绕肿瘤基因组和免疫微环境进行免疫治疗生物标志物转化与开发的策略,并对裕泰抗原围绕肿瘤免疫生物标志物转化与研发成果进行了介绍。

苏小凡博士表示:生物标志物转化研究在新药研发中扮演关键角色,涉及加深对药物与疾病相互关系的理解、精准识别有效的患者群体并开发伴随诊断产品、耐药机制、联合治疗策略等多个方面。免疫治疗的标志物不同于靶向治疗,相对复杂,往往无法用简单的药物靶点标志物来进行疗效预测和患者分层筛选。
基因组标志物
目前PD-L1、MSI 、TMB 是经过临床验证并且被FDA批准用于伴随诊断的生物标志物,但目前被批准的疗效预测生物标志物均存在缺陷。
当PD-L1、TMB、MSI单独作为biomarker时,能够从一定程度上区分获益人群,但都存在较高的假阳性和一定的假阴性率,免疫治疗疗效预测不够精准,被批准的生物标志物在免疫联合治疗中没有相应的疗效预测价值。
以TMB为例,简单通过突变数量算法表征免疫原性并不精准,越来越多高等级循证医学证据表明,除了突变“数量”之外,应该考虑突变的“质量”。
瘤內异质性ITH
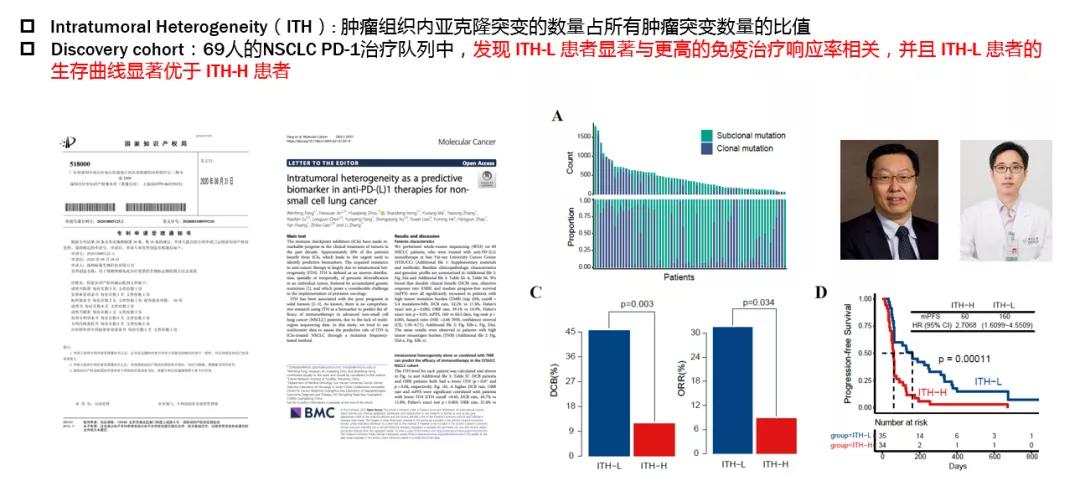
Intratumoral Heterogeneity(ITH)是裕泰抗原自主研发和转化的生物标志物,指肿瘤在生长过程中,经过多次分裂增殖,其子细胞呈现出分子生物学或基因方面的改变,从而使肿瘤的生长速度、侵袭能力、对药物的敏感性、预后等各方面产生差异,是我们难以攻克癌症的因素之一,ITH-H是免疫治疗疗效预测的负向指标。
TMB+ITH
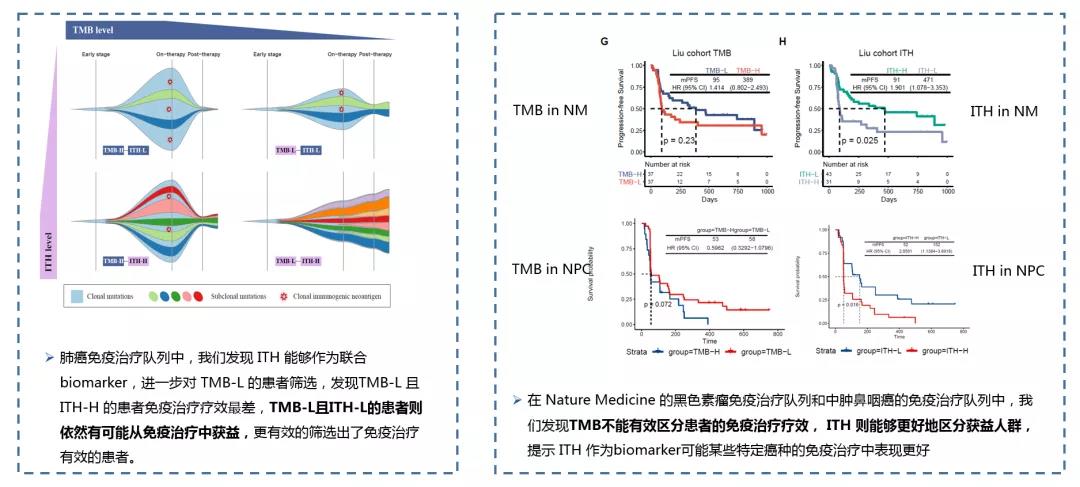
多个独立验证队列数据证明,ITH作为TMB的校正性指标时,两者联用能够更加准确的筛选出对免疫单药敏感的人群,特别是在TMB low人群中筛选回依然能够从免疫治疗获益的患者,在一些TMB进行疗效预测效果不佳的队列中,ITH能够有效的区分免疫治疗获益人群。
接下来,苏小凡博士详细阐述了肿瘤免疫微环境研究在免疫治疗生物标志物开发中的重要性,分别介绍了ICIs联合治疗、TIGIT、 LAG3、双特异性抗体等新型免疫疗法生物标志物研究进展,包括PD-L1、LAG3、MHCII、Claudin 18.2等IHC检测,依然是非常重要的患者筛选生物标志物,即伴随诊断产品开发、转化方向。同时应该在新靶点临床试验中对clonal TMB( ITH+TMB)、TIS (tumer inflamation score)、TILs 等在ICIs治疗中有效的泛癌种生物标志物进行验证。
肿瘤微环境的复杂性决定肿瘤免疫治疗生物标志物需要更多探索,特别是基于多组学平台数据整合分析、生物标志物综合分析、机器学习等新技术手段。裕泰抗原从2020年开始,在高通量测序平台的基础上,陆续引入了国际领先的免疫微环境研究平台,包括基因表达谱、组织病理学、空间转录组、血浆蛋白组学等技术平台,并通过实践总结形成一套完整生物标志物转化研究解决方案。
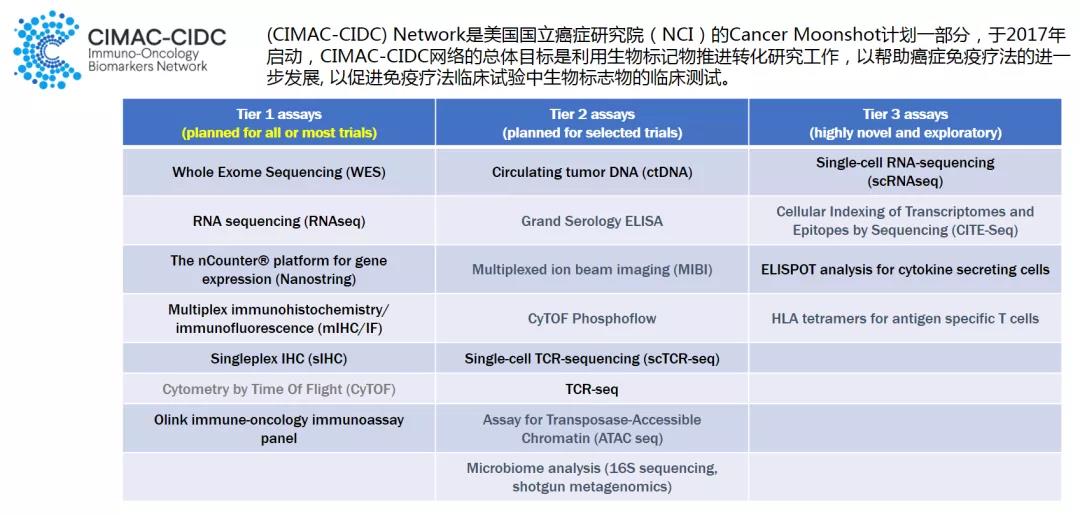
苏博士表示,肿瘤免疫领域生物标志物转化开发,需要在组学数据、生物标志物算法、验证队列等方面有多年的积累。2017年由裕策生物携手詹启敏院士发起,并建立了基于合作、互利、共赢宗旨的抗癌“天梯计划”数据库,旨在积累IO治疗队列数据,加速肿瘤免疫疗法的临床转化。目前合作IO临床研究近50项,积攒了近4500例的病例,基于天梯计划数据平台、裕泰抗原已经开发出多项拥有自主知识产权的肿瘤免疫生物标志物算法。
RNA signature
免疫基因表达谱( Immune gene Signature) 生物标志物开发是一个非常重要的方向、肿瘤组织RNA表达分析可以提供很好的微环境解析、通过早期临床试验回顾性样本进行RNA测序或nCounter IO360 panel检测,生物信息学手段开发免疫基因表达特征(RNA signature),能够更敏感地、特异地筛选免疫治疗获益人群。
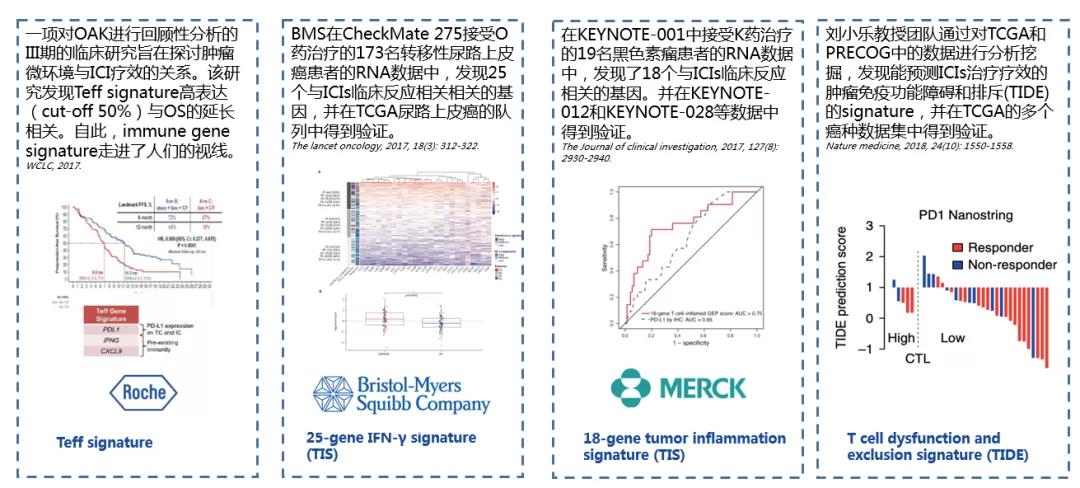
代表性RNA signature:TIS

TIS在多个PD-1单药治疗队列中验证出能够有效筛选响应的患者(黑色素瘤、头颈肿瘤、泛癌肿瘤)。
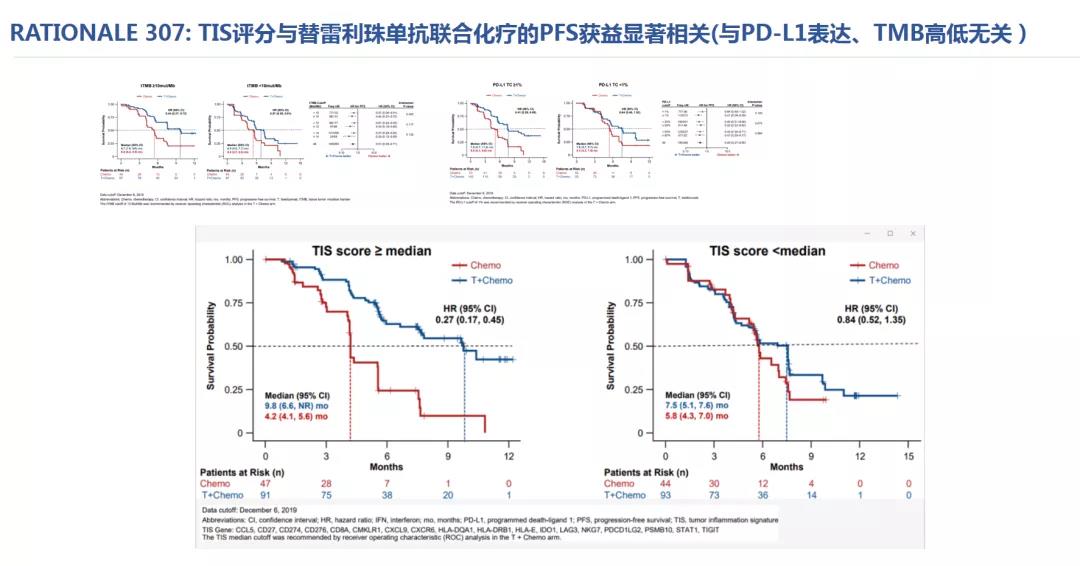
2021年WCLC上报道了替雷利珠单抗+铂类联合NSCLC晚期一线治疗队列(RATIONALE 307)中研究了TMB、 PD-L1表达、TIS三个重要的生物标志物,TIS是唯一能够进行免疫联合化疗疗效预测的生物标志物。
目前已经有多个药企针对药物开发RNA signature并作为患者筛选和入组的生物标志物,裕泰抗原是NanoString在国内唯一授权提供TIS分析实验室。
RNA signature检测与挖掘平台

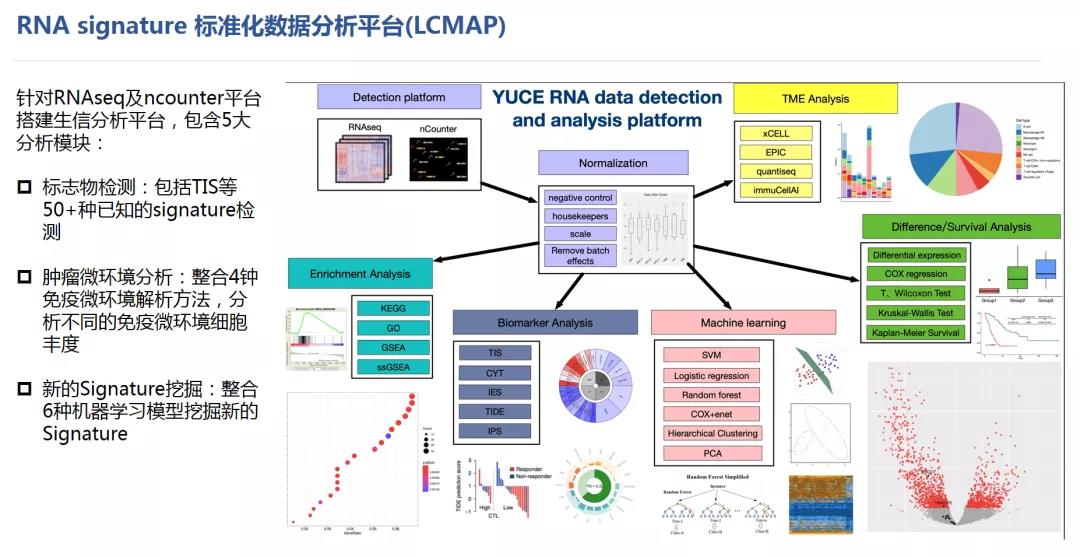
裕泰抗原在RNA signature挖掘领域有着深入研究和丰富的经验,借助于RNA-seq、NanoString nCounter、DSP等RNA检测平台及LCMAP分析平台,能够进行40+ signature的检测、微环境解析、RNA signature开发工作。
蛋白生物标志物
在蛋白生物标志物探索方面,苏博士表示,除了PD-L1等高证据等级的标志物外,其他潜在的疗效标志物也值得关注。
免疫治疗疗效标志物MHC-II
MHC-II (IHC检测)有潜在免疫治疗疗效预测价值,MHC-II 类分子是由6号染色体HLA-D区基因编码,介导外源性抗原的提呈过程,它们提呈外源性抗原多肽分子至Th细胞(helper T cells,辅助性T细胞),参与肿瘤免疫应答反应过程。
既往研究证实MHC-II与黑色素、经典霍奇金淋巴瘤、乳腺癌、鼻咽癌的免疫检查点抑制剂anti-PD(L)1和anti-CTLA4的疗效相关。
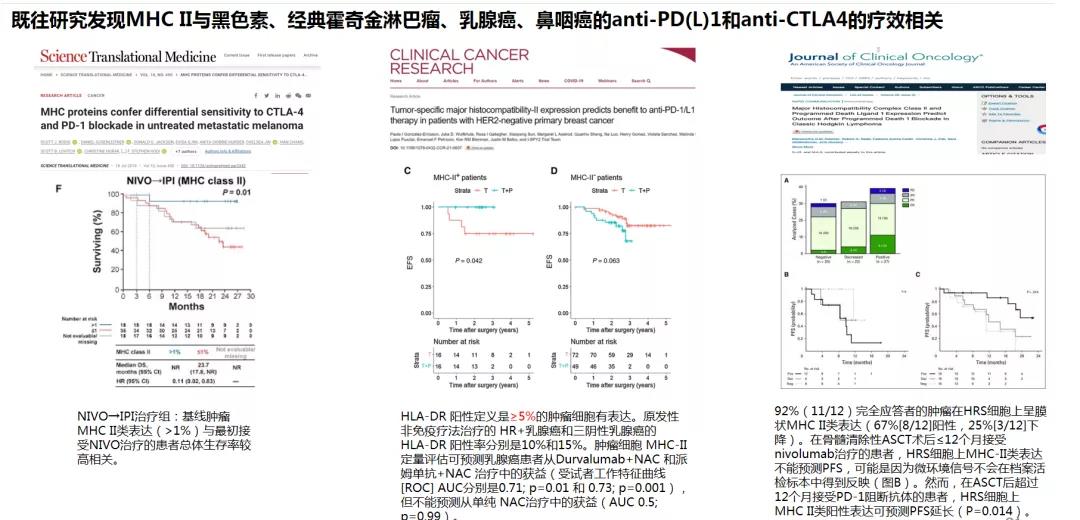
裕泰抗原已经完成MHC-II IHC检测方法的开发,并计划在多个免疫治疗试验队列中进行验证。
mIHC对于免疫治疗疗效评估价值
同时肿瘤免疫微环境的复杂性以及多靶点药物联合用药、双抗药物开发等决定了蛋白标志物探索领域注重多重标志物联合分析。
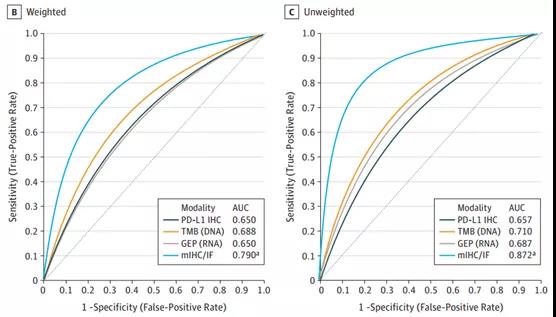
JAMA Oncology meta-analysis 一项研究荟萃分析了2013年-2018年间、56项临床研究、10种+肿瘤样本、8135份的完整临床数据,系统分析肿瘤治疗应答率和PD-L1、TMB、GEP及mIHC/IF等生物标志物的关系,从加权的sROC曲线来看,mIHC/IF(0.79)比PD-L1 IHC(0.65,P <0.001)、GEP(0.65,P= 0.003)和TMB(0.69,P= 0.049)有明显更高的AUC。TMB、GEP的AUC与PD-L1IHC没有显著不同。
mIHC检测的曲线下面积最大,比其它三种标志物的预测价值更高,甚至高于它们共预测的价值,该研究基于大数据证明了mIHC评价免疫治疗有效性强于传统的生物标志物。
蛋白标志物开发整体解决方案
多重免疫组化技术是肿瘤微环境蛋白生物标志物研究的重要工具,苏博士表示,除了技术方面的因素、多重免疫组化marker的选择非常重要。
通常情况下,药物临床试验适用的mIHC panel中marker的选择基于文献报道内容或假设,需要更多证据支持。
裕泰抗原基于空间表达谱蛋白检测技术(DSP)+多重免疫组化技术(mIHC)提供蛋白标志物筛选整体解决方案,在新药研发一期临床或研究者发起临床研究(IIT)进行肿瘤微环境空间蛋白定量分析,根据初步疗效结果相关分析,筛选出差异化表达蛋白,确认蛋白表达空间位置信息,为二期临床试验多色免疫组化panel设计提供重要依据。
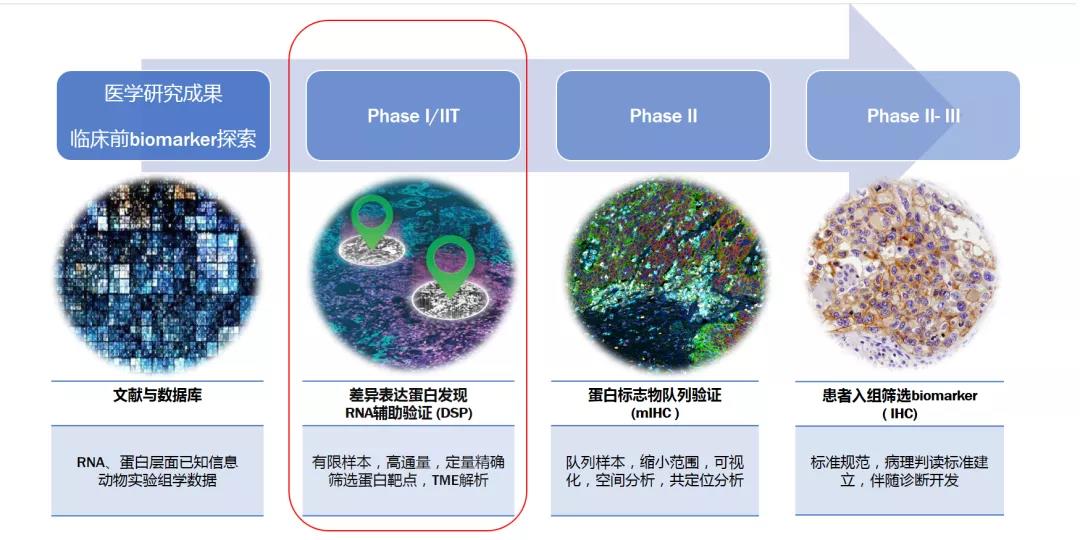
最后,苏博士表示:目前其实并不缺乏药物,而是很多药物没有筛选到合适的治疗人群,我们应该更早、有规划地进行生物标志物转化和开发。比如临床前研究生物标志物研究可以更好理解药物作用机理;临床研究早期阶段(Ia, Ib)尽可能多的进行多组学生物标志物探索;后期Pivotal研究试验中验证能够进行有效患者人群筛选的生物标志物;开发伴随诊断产品提升临床实验成功率。

Copyright©2021
深圳裕策生物科技有限公司 版权所有
粤ICP备16128839号

