 医学检验所地址:
医学检验所地址: 客服邮箱:
客服邮箱: 服务电话:
服务电话: 药企服务专线:
药企服务专线: 网 址:
网 址:
裕泰抗原为客户提供包括新生抗原临床试验生物标志物研究、高质量新生抗原筛选和验证、体内外免疫原性验证、多肽合成与制备、临床试验疗效动态监测等服务。
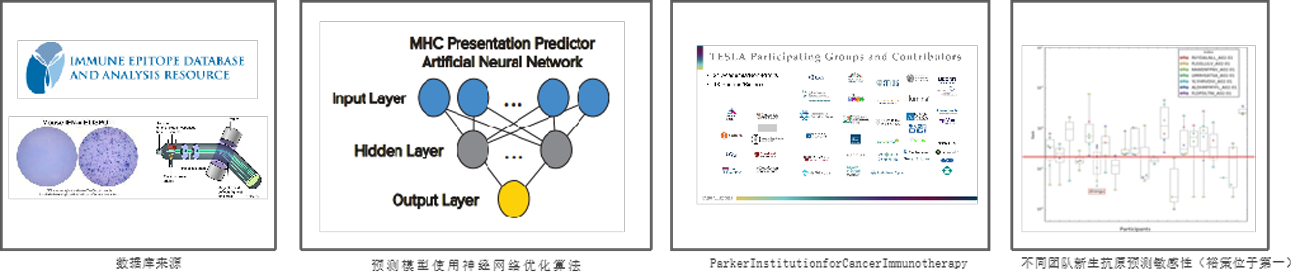
高质量新生抗原筛选和预测
▪ 裕泰抗原拥有自主积累,并经过实验验证的新生抗原阴阳性数据库;
▪ 基于国内最早的真实世界肿瘤免疫数据库“天梯计划”,已建立共有新生抗原数据库;
▪ 自主开发的TruNeo™ 智能机器学习算法,纳入新生抗原传递与识别的生物途径多因素,使新生抗原检测的准确性更高;
▪ 国际肿瘤新生抗原筛查联盟(Tumor Neoantigen SeLection Alliance,TESLA)评测数据显示,TruNeo™ 对新生抗原预测的敏感性达到 87.5%,在所有参评团队中并列第一位,前10位新生抗原验证率达到40%,位居参评团队TOP4
新生抗原多肽免疫原性验证
PDTX(Patient-Derived Tumour Xenografts)人源化小鼠移植所用标本直接来源于人体肿瘤组织,未经过体外培养,稳定地保留了肿瘤的遗传特性、组织学和表型特征,即肿瘤异质性。因此,PDTX 可用于筛选免疫药物敏感或耐药性,试验结果具有较好的临床预见性。
另外,因为 PDTX 在移植过程中较好地保留了肿瘤间质和干细胞成分,使得肿瘤的生长微环境更接近实际情况,还可为肿瘤样本的保存和传代提供大量标本等,能够在临床治疗前对于细胞或者疫苗制剂进行免疫原性的有效性验证,也可用于为小型临床前试验确定合适的样本量和功效评估。
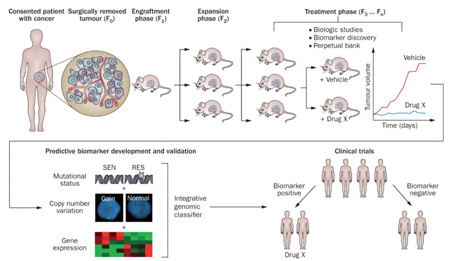
Nat Rev Clin Oncol.2012;9(6):338–350. Published 2012 Apr17. doi:10.1038/nrclinonc.2012.61
如图为 PDTX 的操作流程。获得新鲜的手术组织,将其切成小块,然后植入免疫缺陷小鼠的皮下或腹侧面。包含患者来源材料的小鼠被称为 F0 代,随后的传代小鼠被连续编号(F1,F2,F3等)。一般而言,第三代可以用于药物治疗,但主要还是由 PDTX 在遗传学和组织学方面与患者肿瘤的差异程度决定。
通过 PDTX 试验可以提前预测、验证新生抗原药物的疗效,提高个体化肿瘤新生抗原的治疗有效率。
EliSpot 试验体外验证免疫原性
In vitro 体外免疫原性验证技术——EliSpot
在生物体内,细胞受到刺激后将产生细胞因子(比如IFN-γ),这些细胞因子会被特异性抗体捕获,进而显色形成斑点,斑点数多少代表相应新生抗原具有免疫原性的强弱。此平台将进一步提升裕泰抗原公司筛选新生抗原的精准性。EliSpot对细胞的生物学过程影响很小,且检测细胞的灵敏性更高。基于单细胞水平检测,通过EliSpot实验可从20~30万个细胞中检出1个分泌IFN-γ的细胞,相比Elisa和有限稀释法,EliSpot更加灵敏。
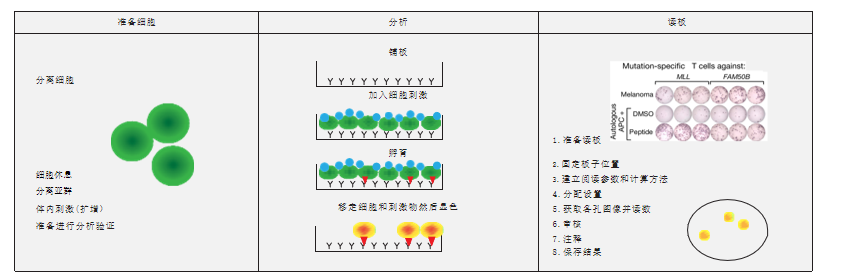
NESt 体外免疫原性验证
EliSpot 可以体外分析哪些新生抗原可以刺激T细胞分泌细胞因子,但是不能检测肿瘤特异性T细胞的TCR。裕泰抗原独有的NESt(Neoantigen Expansion of Specific T cells)验证技术将多肽刺激培养的T细胞的 TCR 测序与生物信息平台整合在一起,以鉴定抗原特异性克隆型扩增。
裕泰抗原 NESt 平台通过对比使用及未用新生抗原多肽刺激的 TCR 库,若能找到频率上升的 TCR,即可表明相应的新生抗原具有免疫原性。
NESt 技术平台不仅可以高通量的验证 TruNeo™ 筛选新生抗原的免疫原性,还可应用于对肿瘤免疫治疗效果进行动态监测*。
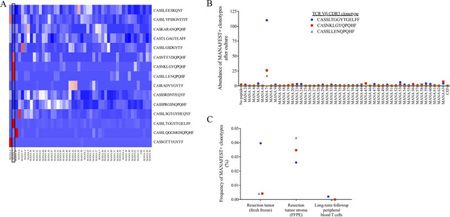
图:NESt分析可识别多个公认的新生抗原,并提供 TCR 序列以跟踪组织和外周血中的抗肿瘤免疫反应。
免疫组库(Immune Repertoire,IR)是指在任何指定时间,某个个体的循环系统中所有功能B细胞和T细胞的总和。用于识别抗原的受体分别为B细胞受体(BCR)和T细胞受体(TCR),在 BCR/TCR 存在一块区域叫互补决定区(Complementary Determining Region,CDR),包含CDR1、CDR2、CDR3,其中 CDR3最高变,在抗原识别中起关键作用,因此 CDR3 基因序列可作为免疫组库多样性的分子标签。
不同B/T细胞淋巴细胞克隆有不同序列或长度的 CDR3 基因,翻译出不同的CDR3多肽序列,从而反映 B/T细胞 BCR/TCR 免疫组库多样性得以恢复和重建。评估和测量免疫系统多样性就为健康状况提供了一种定量指标。研究免疫组库就是测定免疫系统中的 BCR 和 TCR 的基因或 RNA 分子序列,通过使用高通量测序技术,分析编码。通过利用序列比对的位置信息和模式识别方法找到 CDR3 并计算其克隆性和多态性,最后以表格和图形方式输出。
此外,凭借裕泰抗原 NESt 检测平台,对比使用及未用新生抗原多肽刺激 的 TCR 数据和 TCR 序列在不同治疗阶段的表达量变化,可跟踪评估新生抗原相关免疫疗法的疗效。TCR-seq不仅可以用于检测10天肽刺激后的抗原特异性应答,而且可以定量分析应答的多克隆性。
裕泰抗原的新生抗原个体化疗法动态监测平台联合免疫组库和 NESt 技术,可实现对于肿瘤新生抗原个体化临床试验的全程动态监测管理,辅助肿瘤免疫的临床试验提高愈后效果。

Cancer Immunol Res 2018; 6:888-899. Published Online First June 12, 2018.
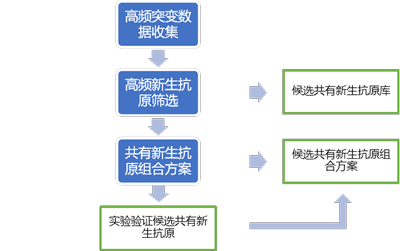
共有新生抗原数据库数据来源:
数据收集:肺腺癌(LUAD)的四个公开研究队列,包括TCGA等
格式解释:
过滤:突变频率(N≥2)&& HLA亲和力(<500nm)&& HLA人群频率(>2%) && exp_CCLE > 1
排序:突变与HLA,分别按人群频率降序排列
记录:MHC-I亲和力最高的短肽序列
待验证:免疫源性(IMMUNO_TYPE)
其他研究队列:
LUSC(肺鳞癌)、STAD(胃癌)、COAD(结直肠癌)、Esophage
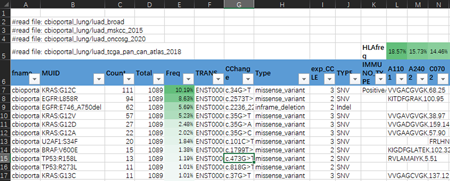
2)共有新生抗原组合方案
a.多个临床试验提及,从研究队列中寻找共有抗原的方法:
Nous-209的早期研究,在MSI-H队列中找到大量重复出现的移码突变
Gritstone基于19个常见突变的临床试验,其专利还提及抗原组合方案降低自体免疫
b.临床试验中,共有新生抗原方案的特点:
新生抗原数量:单一基因(如BRAF V600E) ;或20种抗原组合;或200多种移码突变的组合;
HLA分型:突变对应的HLA分型,或少数高频HLA分型,或针对MHC-II分型的新生抗原;
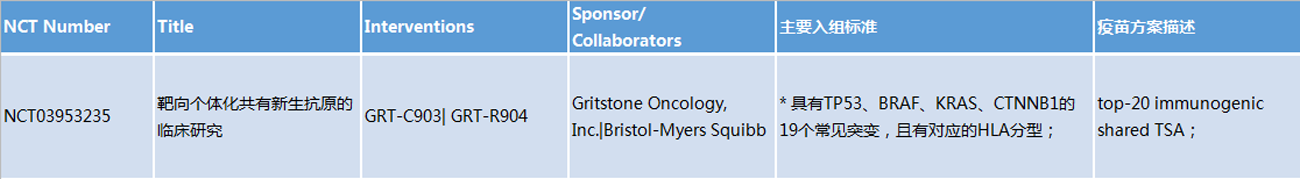
(更多数据请联系客服人员获取)
新生抗原(Neoantigens)是肿瘤细胞里的突变基因产生的正常细胞不表达的肿瘤特异性抗原,能够引起 T 细胞活化。新生抗原在细胞内可被降解成短肽段(抗原表位),通过与 MHC-I 类或MHC-II 类分子高亲和力结合成复合物,并以复合物的形式被 MHC 分子呈递到细胞表面。T 细胞将复合物视为“非己 ” (non-self)物质后活化为效应T细胞,接着效应 T 细胞开始攻击和清除肿瘤细胞。肿瘤抗原有非特异性抗原(tumor-associated antigens,TAA) 与特异性抗原(tumor specific antigen,TSA)之分。非特异性抗原不仅在肿瘤中表达,在正常组织中也有表达,由于中枢耐受,其与 T 细胞的抗原识别亲和力一般都较低。传统的过继细胞治疗、肿瘤疫苗主要是利用肿瘤非特异性抗原来进行实验设计,常面临着疗效差,副作用强等问题。新生抗原是肿瘤特异性抗原,免疫原性较强,被业界认为是免疫治疗的理想之选。
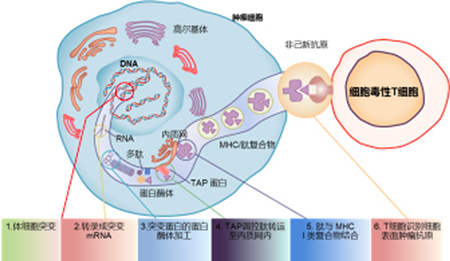
Chabanon RM,etal.Clinical Cancer Research,2016.
国际新生抗原筛查联盟(Tumor Neoantigen SeLection Alliance,TESLA)是由美国著名癌症研究中心 (CRI)和帕克癌症免疫治疗研究所(PICI)联合纪念斯隆凯特琳癌症中心(MSKCC)、MD安德森癌症中心等 30多家新生抗原研究机构组成,旨在通过人工智能算法预测新生抗原,最终形成针对每个患者量身定制的更有效,针对性更强的癌症疫苗。
由帕克癌症免疫疗法研究所(PICI)和癌症研究所(CRI)发起的名为肿瘤新生抗原筛选联盟Tumor Neoantigen Selection Alliance (TESLA) 的科学家们发现了可以更好地预测哪些新生抗原可以激活治疗癌症作用的算法模型和核心参数。TESLA汇聚了包括裕策生物在内的36个顶尖的生物技术,制药,大学和非营利性科研团队,最终发表在《细胞》杂志上,这无疑将催生新一代更有效,更个性化的癌症免疫疗法,也代表着基于新生抗原的个体化免疫疗法新时代已经到来!
科学家们对另一组强调这五个特征的数据模型的癌症样本进行测试时,它可以准确预测出75%的有效新生抗原靶标,并过滤排除98%的无效新靶标。
通过计算分析,该联盟发现了五个特征,这些特征有力地表明了哪些癌症标记最有可能产生免疫反应。这些特征又可以分为两大类:新生抗原在肿瘤细胞上的呈递方式以及免疫系统如何识别新生抗原。
合作客户包括华西医院魏于全院士的500多例非小细胞肺癌 DC 疫苗项目,武汉同济医院马丁院士的 宫颈癌 TILs 治疗,上海细胞集团胆管癌,上00海长海医院消化道肿瘤等,其中有5 项已经进入临床,是国 内最早、最领先的新生抗原领域服务供应商。
以肺癌领域为例:
1.新生抗原 DC 疫苗的癌症辅助治疗(华西医院)

案例1呈现:
1位75岁的男性脑转移小细胞肺癌患者,经历了多种化疗药物耐药,随后使用抗PD-1治疗,但疾病复发。
使用WES和RNA测序评估患者的肿瘤突变,预测潜在新生抗原。选择12个新生抗原肽段合成自体DC新生抗原疫苗。 1.5*10^8 DC疫苗通过皮下输入患者体内,评估治疗疗效。疫苗治疗后10个月,观察到脑转移客观缓解。通过IFN-γ ELISpot分析治疗前后血液中CD4+、CD8+T细胞对12个新抗原表位的应答,评估每个表位的免疫原性。预测的新抗原表位中有75%的新表位引起了CD4+/CD8+T细胞的免疫应答,表明该患者中,T细胞针对多个预测的新表位产生了应答。
案例2:

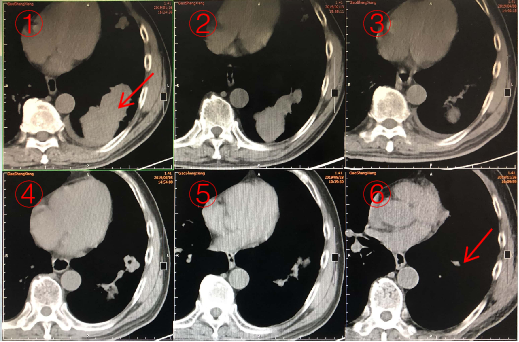

研究目的:评估基于新生抗原疫苗联合ICI在一例晚期肺鳞癌患者中的疗效
案例:1位接受了化疗、放疗、靶向、抗血管生成治疗的的晚期肺鳞癌(68岁,男性)
方法:全外显子测序,检测突变,预测新生抗原;选择17个新生抗原肽段合成自体DC疫苗。1.38*108 DC疫苗输入患者体内(day 1、7、15、22、30)联合抗PD-1(4mg/kg,followed by 2mg/kg biweekly)
通过IFN-γ ELISpot分析血液中CD4+、CD8+T细胞对17个新抗原表位的应答,评估每个表位的免疫原性
结果:
疫苗治疗后10个月,发现患者达到部分缓解。
预测的新生抗原表位中有64.71%(11/17)的新表位引起了CD4+/CD8+T细胞的免疫应答
结论:
DC新生抗原疫苗联合PD-1抑制剂在经多线治疗的肺癌患者中安全,耐受
新生抗原疫苗在体外引起了T细胞免疫应答
生物信息预测算法有助于筛选高质量新生抗原
该研究为晚期肺癌测试新生抗原疫苗联合疗法提供了研究框架
案例3:
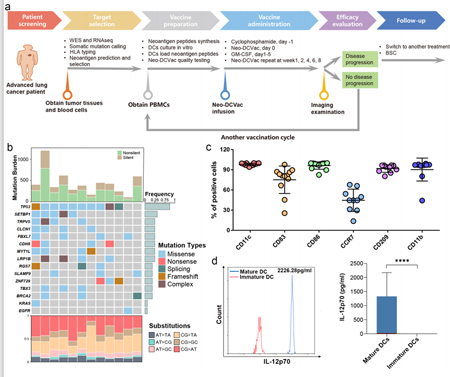
入组21例经多线治疗晚期肺癌患者,其中可接受疫苗治疗的12例:
通过WES+RNA测序,预测和筛选新生抗原;
自体PBMC体外培养,诱导分化为DC细胞,将合成的新生抗原肽段加载至DC,制备新生抗原DC疫苗;
疫苗注射(皮下)及疗效评估,每个治疗周期后(包含5次)未进展再次疫苗治疗,进展采用其他治疗方式。
结论:
TP53在患者中的突变频率最高,仅一位患者携带EGFR突变
生产制备的DC疫苗中,表达成熟DC表型标志物、抗原呈递标志物的DC细胞平均比例高
Copyright©2021
深圳裕策生物科技有限公司 版权所有
粤ICP备16128839号

