
导读
随着NGS测序的发展,使用机器学习AI算法对NGS数据进行数据挖掘,发现生物标志物和构建AI预测模型,已经逐渐成为主流的研究方法。另外,近几年来随着肿瘤免疫治疗的快速发展,在临床治疗和科学研究中,肿瘤微环境都受到越来越多的关注。而肿瘤微环境的复杂性决定肿瘤免疫治疗生物标志物需要更精细的探索,尤其需要结合多组学平台数据整合分析、生物标志物综合分析、机器学习等新技术手段。2021年11月,山东第一医科大学第一附属医院王俊教授与裕策生物/裕泰抗原合作的研究成果Identification of a prognostic immune-related signature for small cell lung cancer发表于Cancer Medicine (IF=4.452)杂志。裕策生物/裕泰抗原负责了本研究中生物信息数据分析和机器学习模型搭建工作。
背景
小细胞肺癌(small cell lung cancer, SCLC)占肺癌总数的10%-15%。其特点是恶性程度高、病情进展快、预后差、难治性,大约70%的患者在确诊时就已经处于广泛期。在过去的30余年中,SCLC以化疗和放疗为主的传统治疗策略,中位总生存期只有8-13个月。而在过去的几年中,一些临床试验评估了以细胞毒性T淋巴细胞相关抗原4(CTLA-4)和程序性死亡受体1(PD-1)/程序性死亡配体-1(PD-L1)抑制剂为主的检查点抑制剂在SCLC患者中的治疗效果,并展示了良好的生存前景。本研究基于转录组数据进行基因表达和肿瘤微环境状态分析,旨在增加对SCLC免疫和肿瘤微环境的认知,发现SCLC免疫相关的标志物,为未来SCLC治疗方案的选择提供更多参考。
研究结果解读
模型搭建
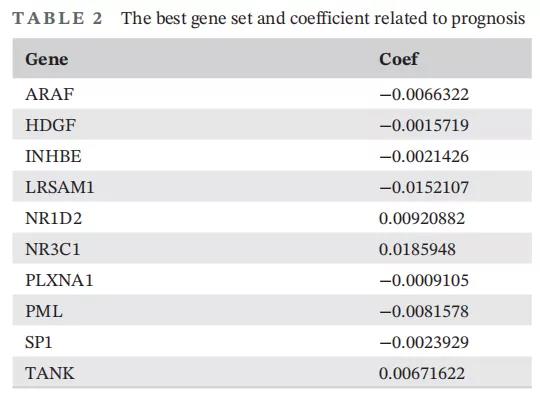
研究中下载了之前研究中公开发表的RNAseq数据,用从ImmPort数据库下载的2498个免疫相关基因作为基础进行数据筛选。通过Cox比例风险回归算法筛选出77个与预后显著相关的基因后,最后基于弹性网络惩罚的多因素Cox比例风险模型进行模型训练,得到最具有小细胞肺癌患者预后预测能力的10基因风险模型(NR3C1、NR1D2、TANK、ARAF、HDGF、INHBE、LRSAM1、PLXNA1、PML、SP1),该模型对患者的生存期显现出强大的预测价值。为了鉴定这10个基因参与的生物学过程和通路,进行了GO富集分析和KEGG通路分析。结果表明,这些基因参与了急性髓系白血病(p=0.04)、TGF-β信号通路(p=0.04)、内分泌耐药性(p=0.04)和甲状旁腺激素的合成、分泌和作用(p=0.04)。
生存分析
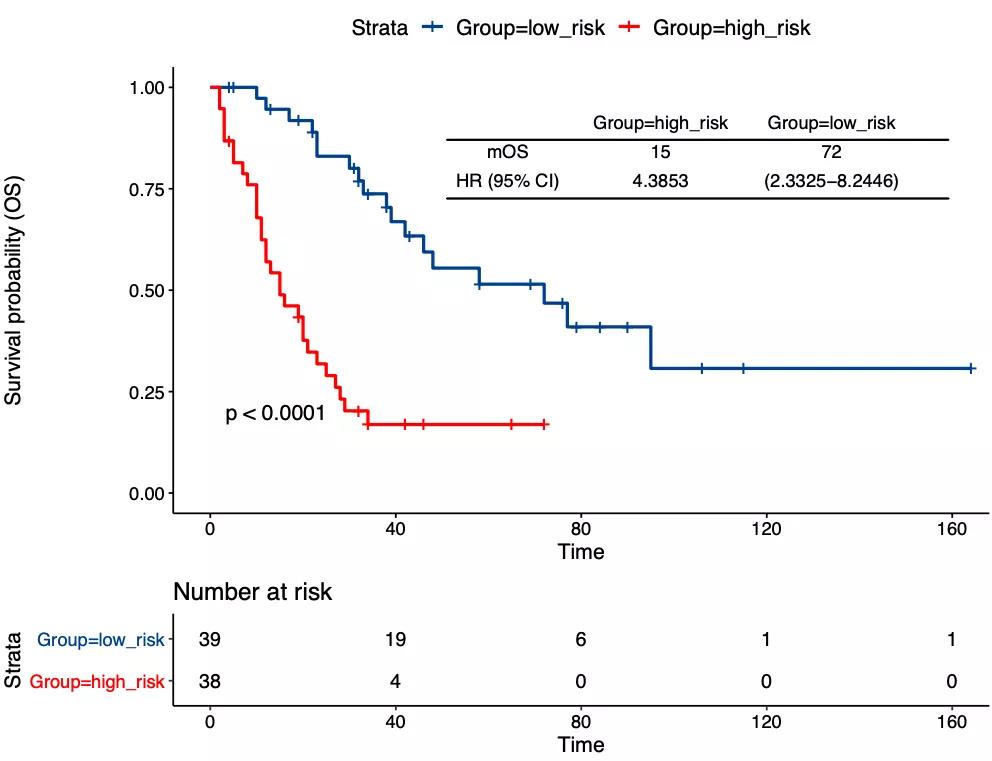
根据10个基因的表达水平和系数计算每个SCLC患者的风险评分,并根据风险评分将患者分为高风险组(High risk)和低风险组(Low risk)。Kaplan-Meier生存分析显示低风险组的SCLC患者的OS明显优于高危组的OS(HR=3.71, 95%CI:1.25-11.05,p=0.012),验证了风险模型的预后预测性能。
免疫微环境分析
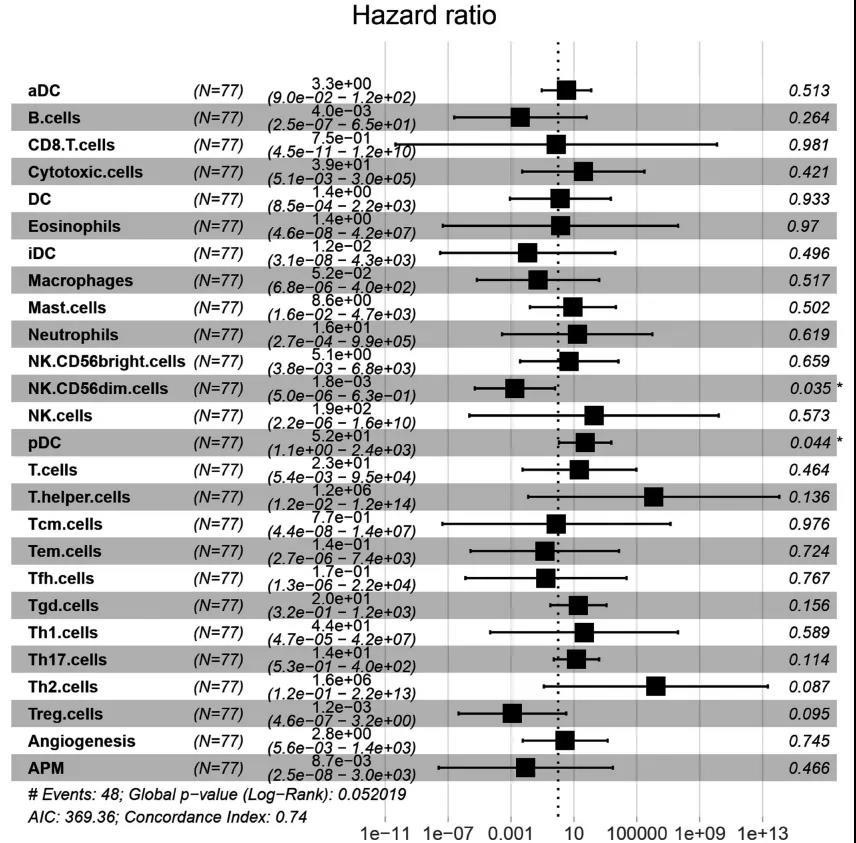
肿瘤浸润免疫细胞的风险打分情况
采用ssGSEA富集算法计算小细胞肺癌患者26个免疫细胞的丰度,并采用Cox回归分析免疫细胞丰度与总生存期(OS)的关系。发现CD56dim NK细胞的丰度是SCLC患者生存的有利预后因素(p=0.035),而浆细胞样树突状细胞(pDC)的丰度是SCLC患者生存的不良预后因素(p=0.044)。其他免疫细胞亚群,包括CD8+T细胞、巨噬细胞或T细胞,与患者总生存期没有显著相关性。
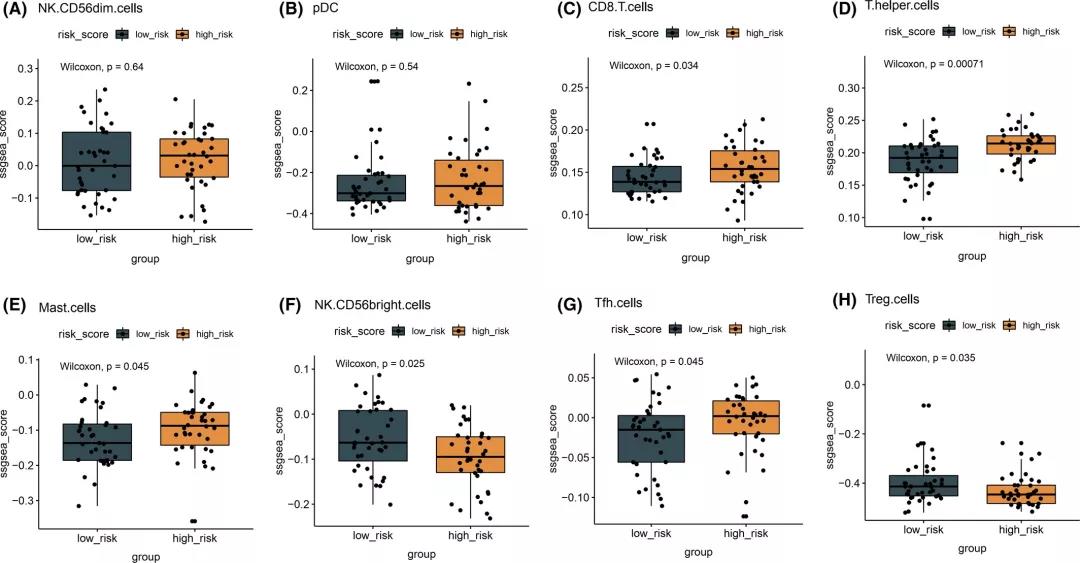
另外研究中比较了高风险评分与低风险评分组的肿瘤微环境差异。发现与小细胞肺癌患者预后相关的CD56dim NK细胞和pDC在不同风险评分组之间无显著差异。而不同风险评分组之间的CD8+T细胞,T 辅助细胞(T helper),肥大细胞(Mast cell),NK CD56bright NK细胞,调节T细胞(Treg)和滤泡辅助性T细胞(Tfh)的丰度存在显著差异,这表明风险评分能反应出和肿瘤微环境密切相关的免疫细胞丰度状态。
临床信息关联分析
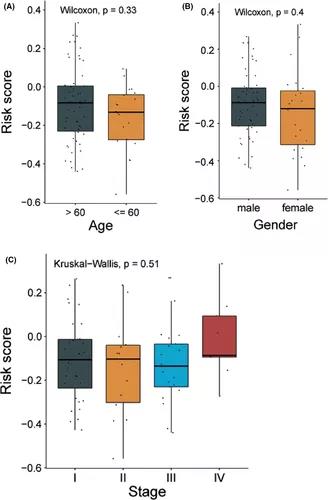
此外,对患者临床信息进行生存风险分析,发现SCLC患者的性别是生存风险的良好预后因素,女性SCLC患者的生存风险显著降低(HR=0.32,95%CI:0.14–0.70,p=0.004),这可能是因为大部分男性通过吸烟导致的罹患小细胞肺癌。同时肿瘤分期是患者不良预后因素(HR=1.42,95%CI:1.07–1.9,p=0.014)。通过统计检验发现患者不同性别,不同分期的分组之间的风险评分没有显著差异,这说明风险评分是和性别、肿瘤分期分别独立的预后因素。
小结
本研究中使用机器学习AI算法基于转录组数据构建了一个免疫风险评分模型,可用于预测小细胞肺癌患者预后。并发现了10 个特征基因富集于生长因子活性和免疫相关的TGF-β信号通路。并通过进行肿瘤微环境状态分析,发现肿瘤微环境中CD56dim NK细胞和pDC细胞的丰度与小细胞肺癌患者预后相关,同时发现风险评分模型能反应出和肿瘤微环境密切相关的免疫细胞的丰度状态,如CD8+T细胞,T 辅助细胞(T helper),肥大细胞(Mast cell),NK CD56bright NK细胞,调节T细胞(Treg)和滤泡辅助性T细胞(Tfh)等。最终,本研究增加了对SCLC免疫和肿瘤微环境的认识,发现了SCLC免疫相关的标志物,为未来SCLC治疗方案的选择提供更多参考。
DIA壁报
裕策生物/裕泰抗原从2020年开始,在高通量测序平台的基础上,陆续引入了国际领先的免疫微环境研究平台,包括基因表达谱、组织病理学、空间转录组、血浆蛋白组学等技术平台,并结合实践开发了基于AI进行生物标志物挖掘的数据分析平台,形成一套AI与算法驱动的生物标志物转化研究解决方案。例如,在今年"国际药物信息大会(DIA)中国年会"上,裕策生物/裕泰抗原参展的壁报中,展示了一项使用机器学习算法挖掘免疫治疗标志物(免疫排斥评分、IES)的研究,该壁报被DIA授予了“最有创新价值壁报”的嘉奖,肯定了裕策生物/裕泰抗原在免疫治疗生物标志物研发的实力,同时显示了机器学习在生物标志物研发中的潜力。
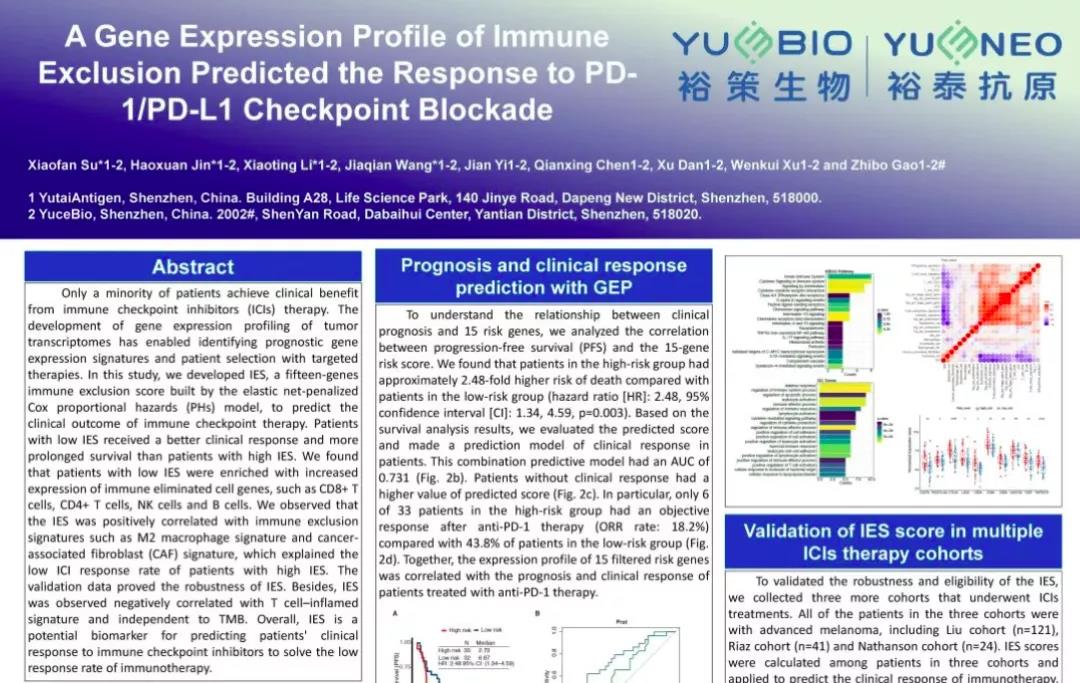
DIA壁报
DIA参考链接:https://mp.weixin.qq.com/s/rU6lw8oz8AT4osNqXEy45g
参考文献:
Xie Q, Chu H, Yi J, et al. Identification of a prognostic immune‐related signature for small cell lung cancer[J]. Cancer Medicine, 2021.doi.org/10.1002/cam4.4402.
Copyright©2021
深圳裕策生物科技有限公司 版权所有
粤ICP备16128839号

